חידושים הקשורים לאלקטרודות ולקוצב (IPG)
הגורם החשוב ביותר ביותר להצלחת הטיפול בקוצב מח הוא מיקום מדויק של האלקטרודות בגרעין המטרה במוח, בדרך כלל אזור שאחראי על תפקוד מוטורי בגרעין הסאב-תלמי (STN- SUBTHALAMIC NUCLEUS ).
באופן אידאלי השדה החשמלי הנוצר סביב האלקטרודה המושתלת משפיע רק על מבנים המעורבים במחלת פרקינסון וניתן לשפר ללא תופעות לואי את האיטיות, הנוקשות, רעד ועוד. אולם, בסמוך לחלק המוטורי של גרעין הSTN נמצאים אזורים נוספים המשפיעים על תפקודים מוחיים חשובים אחרים, ולכן במידה והאלקטרודות לא ממוקמות במרכז האזור המוטורי של הSTN הקיצוב החשמלי עלול לגרום בין השאר לתופעות לואי לא רצויות כגון קושי בדיבור או שינויים במצב הרוח עקב השפעה של השדה החשמלי על אזורים סמוכים שמחוץ לאזור המטרה.
לכן, לפני ביצוע הניתוח נעשות בדיקות הדמיה מיוחדות באמצעות MRI ברזולוציה גבוהה על מנת לזהות את גרעיני המטרה בעומק המח ולתכנן את מסלול הכנסת האלקטרודה בניתוח. בנוסף, על מנת לוודא את מיקום האלקטרודות בזמן אמת, מבוצעים בזמן הניתוח רישומים של הפעילות העצבית מעומק המח באמצעות אלקטרודות עדינות (micro-electrodes ) אשר מסוגלות לרשום פעילות של נוירונים בודדים. רישומים אלו עוזרים לזהות פעילות מוחית האופיינית לגרעין הSTN במחלת פרקינסון.
כאשר האלקטרודה ממוקמת בצורה אופטימלית במח נוכל לשלוט ביתר קלות בתסמינים הפרקינסונים של נוקשות, איטיות, רעד וכדומה ובאופן תיאורטי ללא תופעות לואי.
לאחר הניתוח המטופל מגיע לרב לנוירולוג מומחה להפרעות תנועה ולקיצוב DBS על מנת לתכנת את הקוצב כל שהשדה החשמלי יכלול באופן מרבי את אזור המטרה המעורב בתסמינים המפריעים ויכלול כמה שפחות אזורים שקיצובם יכול לגרום לתופעות לואי. הטווח בין עוצמת בו מושגת השפעה טובה על התסמינים לעוצמת גירוי בה מופיעות תופעות לואי נקרא "החלון הטיפולי" (מעין חלון הזדמנויות לטיפול) .
בשנים האחרונות חלה התקדמות טכנולוגית משמעותית בתחום הDBS ובין השאר פותחו טכנולוגיות שמאפשרות לנו להגדיל את החלון הטיפולי כלומר מאפשרות לנו ביתר קלות לקצב את הרקמה הרצויה ולהגיע לשליטה טובה בתסמינים הפרקינסונים, תוך הקטנה של תופעות הלוואי.
אציין כעת 2 טכנולוגיות עיקריות שהגיעו לישראל.
- אלקטרודות רב כיווניות ( Directional Leads )
- טכנולוגיית חישה/ חוג פתוח. (Sensing )
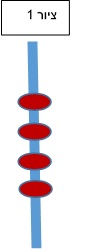
1. אלקטרודות רב כיווניות: האלקטרודות הקלאסיות בהן משתמשים לקיצוב בפרקינסון מכילות 4 מגעים זהים בצורת טבעת (360 מעלות) שממוקמים אחד מעל השני במרווחים קבועים. מתוכם מפעילים לרב מגע אחד או שניים שממוקמים בתוך אתר המטרה. כאשר מפעילים את המגעים הזרם החשמלי מתפשט בצורה כדורית (ספרית) לכל הכוונים (ציור 1). במצב זה אם האלקטרודה מוסטת במילימטר או שניים ממרכז המטרה, הרקמה שעליה נשפיע באמצעות הזרם החשמלי עלולה לכלול גם אזורים סמוכים שקיצובם יכול לגרום לתופעות לואי.
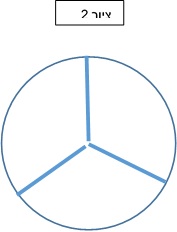
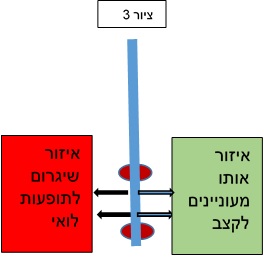
האלקטרודות הרב כיווניות בנויות כך ששני המגעים האמצעיים שלהן מחולקים ל-3 תת- מגעים (ציור 2 ) כך שניתן לשלוט ולהפעיל כל אחד מהם בנפרד. באופן זה, ניתן לעצב את השדה החשמלי שנוצר שכעת אינו חייב להיות כדור סימטרי אלא יכול לסטות לכיוון מסוים (ציור 3). הקיצוב תוך שימוש באלקטרודות הרב כיווניות נקרא באנגלית STEERING מלשון הגה , ניתן לסובב את השדה החשמלי כמו הגה במכונית שמאפשר לי לפנות לכוונים שונים (ציור 2 ).
למעשה, במחקרים מוקדמים שבדקו השפעה של הפעלת שדה כדורי (3 מגעים שיוצרים 360 מעלות) לעומת הפעלה של שדה כווני על ידי שימוש במגע אחד או שניים בלבד מתוך אותם השלושה שבאותו גובה, מצאו שהפעלת שדה חשמלי על ידי מגע אחד או שניים (פחות מ360 מעלות), מצאו כי הפעלת שדה חשמלי אפשרה קיצוב על יעילות טובה יותר ושכרוך בפחות תופעות לואי. כלומר, התקבל חלון טיפולי היה גדול יותר על ידי שימוש בטכניקת קיצוב כיוונית.
2. טכנולוגיית חישה/חוג פתוח:
כפי שהוזכר בתחילה, על מנת לוודא מיקום אלקטרודות במהלך הניתוח לוקחים בחשבון 2 ממדים. ממד אנטומי- על ידי שימוש בהדמיה מתקדמת לפני ואחרי הניתוח וממד פיזיולוגי/תפקודי- רישום וזיהוי של פעילות תאי מח בעלת מאפיינים מסוימים של מחלת פרקינסון באזור המטרה בו מעוניינים להשתיל את האלקטרודות. בחולי פרקינסון הפעילות המוחית בגרעין STN מתאפיינת בפעילות פתולוגית בתדר "גלי בטא" (20-30 הרץ) וכאשר מזהים אותה בזמן הניתוח, אנו יודעים שהאלקטרודה ממוקמת באזור המטרה.
עד לאחרונה, לא ניתן היה להמשיך ולרשום את הפעילות המוחית באזור המקוצב לאחר ההשתלה של האלקטרודות הקבועות.
בשנים האחרונות ,חוקרים פיתחו טכנולוגיה שמאפשרת להמשיך ולרשום פעילות מוחית גם מהאלקטרודות הקבועות המושתלות במח ומחוברות לקוצב הDBS . אחד מהאתגרים היה להתגבר על רעשי רקע ובכל זאת לקבל אותות בזמן אמת ותוך כדי פעילות של מטופלים.
בשנה האחרונה הטכנולוגיה הנ"ל אושרה לשימוש קליני וכיום יש לנו אלקטרודות שמחוברות לקוצב ומסוגלות להקליט לפרקי זמן מסוימים את פעילות גלי הבטא שמבטאים את הפעילות ה"פרקינסונית" במח. המטרה היא שעל ידי שימוש ברישומים של פעילות המח בזמן אמת, נוכל לגלות באילו מבין 4 המגעים בקצה האלקטרודה ממוקם בצורה האופטימלית בתוך גרעין המטרה. בנוסף, נוכל לבדוק את השפעת הקיצוב על הפעילות הפתולוגית ה"פרקינסונית" במח ולהתאים את הקיצוב כך ש ישנה אותה בחזרה לתצורה פיזיולוגית (תקינה). עד היום ההחלטות הללו היו מתקבלות על ידי בדיקה קלינית של המטופל והערכה של מידת הנוקשות, איטיות ורעד. מידע שמתקבל מתוך המח עצמו יכול לעזור ולכוון אותנו טוב יותר ומהר יותר לפרמטרי הקיצוב המועדפים תהליך שיכול חודשים מספר.
יש לציין, כי בשלב זה הטכנולוגיה עדיין חדשה, ישנן עדיין שאלות טיפוליות רבות לא פתורות ולא קיימים אלגוריתמים טיפוליים סדורים לשימוש קליני ולקבלת החלטות הנגזרות מהמידע המתקבל.
החזון הוא, שבעתיד הקוצב עצמו יוכל לעבד את הקלט מהאלקטרודות המושתלות ולהתאים את הקיצוב בזמן אמת לצרכי המטופל בצורה אופטימלית, תוך שילוב שתי הטכנולוגיות- חישה וכיווניות.